Anvisa aprova Mounjaro para crianças a partir de 10 anos com diabetes tipo 2
Decisão da agência reguladora brasileira, publicada em 22Abr26, autoriza o medicamento da Eli Lilly para pacientes de 10 a 17 anos. Estudo clínico publicado na revista The Lancet mostrou redução média de 2,2% da hemoglobina glicada.
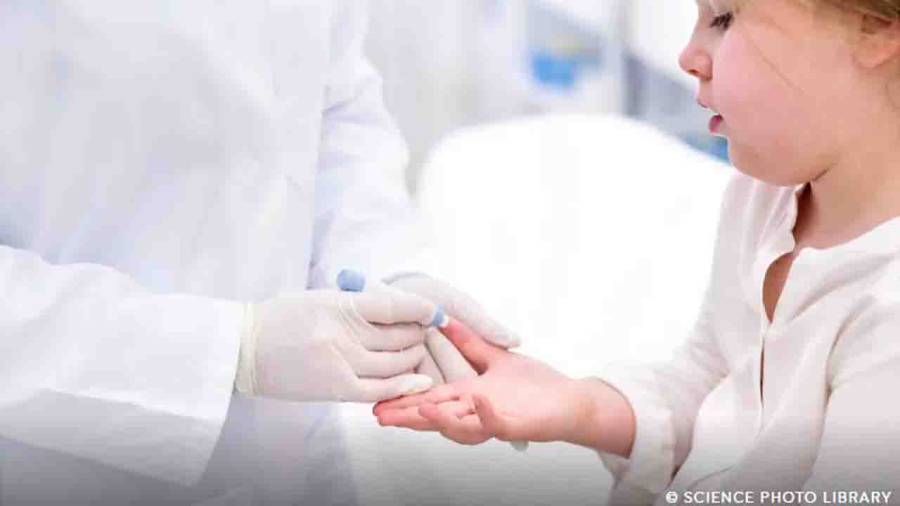 Mounjaro (tirzepatida) é o primeiro agonista dual GIP/GLP-1 aprovado para uso pediátrico no Brasil. Foto: science photo library.
Mounjaro (tirzepatida) é o primeiro agonista dual GIP/GLP-1 aprovado para uso pediátrico no Brasil. Foto: science photo library. A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso da tirzepatida, comercializada como Mounjaro, para o tratamento de diabetes tipo 2 em crianças e adolescentes de 10 a 17 anos. A decisão, publicada em 22 de abril de 2026, amplia a indicação de um medicamento que já era autorizado no país para adultos com a doença.
Com a nova autorização, o Mounjaro passa a ser o primeiro fármaco da classe dos agonistas duplos dos receptores GIP/GLP-1 liberado para uso pediátrico no Brasil. Esses medicamentos atuam em hormônios relacionados ao controle da glicose e do apetite, ajudando a reduzir os níveis de açúcar no sangue.
Quer receber notícias políticas em primeira mão? Clique aqui e entre no nosso canal do WhatsApp.
O cenário no Brasil -
De acordo com dados citados pela Anvisa na decisão, cerca de 213 mil adolescentes vivem com diabetes tipo 2 no Brasil, além de mais de 1,4 milhão com pré-diabetes. A doença do tipo 2 em jovens tem incidência crescente nas últimas décadas, impulsionada principalmente pelo aumento global da obesidade.
Nos Estados Unidos, a incidência geral de diabetes tipo 2 em crianças e adolescentes quase dobrou em 15 anos, passando de 9,0 para 17,9 casos por 100 mil pessoas por ano entre 2002-2003 e 2017-2018.
O estudo SURPASS-PEDS: o que a ciência diz?
A autorização da Anvisa se baseou nos resultados do estudo clínico de fase 3 SURPASS-PEDS, publicado na revista The Lancet em setembro de 2025.
Como foi o estudo?
O ensaio clínico multicêntrico, randomizado, duplo-cego e controlado por placebo incluiu 99 participantes com idade entre 10 e 18 anos com diabetes tipo 2 não adequadamente controlado por metformina, insulina basal ou ambos. O estudo foi conduzido em 39 centros distribuídos por oito países: Estados Unidos, Austrália, Brasil, Índia, Israel, Itália, México e Reino Unido.
Na linha de base (início do estudo), os participantes tinham hemoglobina glicada (HbA1c) média de 8,04%, índice de massa corporal (IMC) médio de 35,4 kg/m², peso médio de 96,6 kg e tempo médio de diagnóstico de diabetes de 2,4 anos.
Os pacientes foram divididos aleatoriamente em três grupos: tirzepatida 5 mg, tirzepatida 10 mg ou placebo, aplicados uma vez por semana. O objetivo primário era medir a variação da HbA1c após 30 semanas. O estudo teve ainda uma extensão aberta de 22 semanas (totalizando 52 semanas), na qual todos os participantes passaram a receber tirzepatida.
Resultados principais -
Controle glicêmico: Após 30 semanas, o grupo tratado com tirzepatida (doses agregadas) apresentou redução média da HbA1c de 2,2% em relação ao valor basal (8,05%), enquanto o grupo placebo teve aumento de 0,05% (diferença estatisticamente significativa com p<0,0001).
Na dose de 10 mg, 86,1% dos participantes alcançaram a meta de HbA1c ≤6,5% — o alvo recomendado pela American Diabetes Association. No grupo placebo, apenas 27,8% atingiram essa meta.
Redução de peso e IMC: A dose de 10 mg reduziu o IMC em 11,2% na média, contra apenas 0,4% no placebo. A circunferência da cintura reduziu em média 10,28 cm no grupo tratado.
Benefícios metabólicos adicionais: O tratamento com tirzepatida também promoveu reduções significativas em triglicerídeos (redução de 31,8%), colesterol total (redução de 11%) e colesterol LDL (redução de 9,1%). Os efeitos benéficos foram sustentados ao longo das 52 semanas do estudo.
O que dizem os especialistas?
A pesquisadora principal do estudo, Tamara Hannon, MD, diretora do Programa de Diabetes Clínico da Universidade de Indiana, afirmou :
"Os jovens vivendo com diabetes tipo 2 frequentemente enfrentam um curso mais agressivo da doença e, em muitos casos, os tratamentos de primeira linha como metformina e insulina basal falham em controlar adequadamente a hemoglobina glicada. Os resultados do SURPASS-PEDS mostram que o Mounjaro produziu melhorias significativas e clinicamente relevantes no açúcar no sangue, IMC e glicemia de jejum em pacientes pediátricos. Esses resultados oferecem uma oportunidade promissora para ajudar a mudar a trajetória de saúde de longo prazo dos jovens que vivem com essa condição complexa."
Segurança e efeitos colaterais.
Eventos adversos mais comuns -
O perfil de segurança da tirzepatida em adolescentes foi geralmente consistente com o observado em estudos com adultos. Os eventos adversos mais comuns foram gastrointestinais, ocorrendo predominantemente durante a fase de aumento da dose.
No grupo tratado com tirzepatida (doses agregadas), a diarreia ocorreu em 25% dos participantes, contra 6% no grupo placebo. Náusea foi relatada em 20% dos pacientes tratados, enquanto no placebo chegou a 9%. Vômito apareceu em 14% dos que usaram o medicamento, contra apenas 3% no grupo de controle. Dor abdominal foi observada em 9% dos tratados com tirzepatida e em 3% dos que receberam placebo. Todos os eventos foram classificados como de gravidade leve a moderada.
Hipoglicemia -
Não foram observados episódios de hipoglicemia grave no estudo. A hipoglicemia de nível 2 (glicemia abaixo de 54 mg/dL) ocorreu em 15,4% dos participantes tratados com tirzepatida contra 5,9% no placebo — uma taxa consistente com a observada em outros estudos sobre diabetes tipo 2 de início jovem.
Interrupções do tratamento -
As taxas de descontinuação do tratamento devido a eventos adversos foram baixas: 6% no grupo de 5 mg, 0% no grupo de 10 mg, e 3% no agregado de doses, contra 0% no placebo.
Alertas importantes (boxed warning).
O medicamento possui alerta de caixa preta, o mais grave da FDA, devido à ocorrência de tumores de tireoide em ratos em estudos com a medicação. De acordo com a bula do medicamento, é desconhecido se o Mounjaro causa tumores tireoidianos ou carcinoma medular de tireoide (MTC) em humanos.
Contraindicação absoluta: pessoas com histórico pessoal ou familiar de carcinoma medular de tireoide, ou com síndrome de Neoplasia Endócrina Múltipla tipo 2 (MEN 2), não devem utilizar o medicamento.
Outros efeitos adversos graves possíveis -
Segundo a bula do medicamento, outros eventos adversos graves que requerem atenção médica incluem inflamação do pâncreas (pancreatite) com dor abdominal severa que não cessa, desidratação levando a problemas renais, problemas graves no estômago, problemas na vesícula biliar, alterações na visão (em pacientes com retinopatia diabética) e reações alérgicas graves.
Posologia e administração para crianças -
A dosagem para crianças segue um esquema de ajuste gradual ("step-up") para que o organismo se adapte à medicação. A dose inicial é de 2,5 mg, aplicada uma vez por semana, durante 4 semanas. Após completar as 4 semanas iniciais, aumenta-se para 5 mg uma vez por semana. A dose máxima para crianças é de 10 mg uma vez por semana, que não deve ser excedida.
O medicamento é injetado sob a pele (subcutâneo) no abdômen, coxa ou parte de trás do braço, podendo ser administrado em qualquer horário do dia, com ou sem refeições. Recomenda-se alternar o local da aplicação a cada semana para evitar problemas na pele.
Importante: Crianças não devem se autoinjetar o Mounjaro KwikPen. A aplicação deve ser supervisionada por um adulto responsável.
Contraindicações e precauções -
Não deve ser usado por crianças que tenham: histórico pessoal ou familiar de carcinoma medular de tireoide (MTC), síndrome de Neoplasia Endócrina Múltipla tipo 2 (MEN 2), ou histórico de reação alérgica grave à tirzepatida ou a qualquer componente do medicamento.
Atenção especial para crianças com: problemas no pâncreas, problemas gástricos graves (como gastroparesia), retinopatia diabética, ou cirurgias programadas e procedimentos com anestesia.
Interação com anticoncepcionais orais: O medicamento pode reduzir a eficácia de anticoncepcionais orais (pílula anticoncepcional). Para meninas que utilizam esse método contraceptivo, recomenda-se o uso de um método contraceptivo adicional ou alternativo por 4 semanas após o início do tratamento e por 4 semanas após cada aumento de dose.
O que isso significa na prática?
Na prática clínica, a nova indicação permite que médicos considerem a tirzepatida como alternativa terapêutica em crianças e adolescentes com diabetes tipo 2 nos casos em que outras terapias não foram suficientes para controlar a glicemia. O tratamento deve ser individualizado e rigorosamente acompanhado por especialista, já que envolve uma população em fase de desenvolvimento e potencialmente mais vulnerável.
A autorização da Anvisa consolida o Brasil entre os primeiros países a liberar o uso pediátrico do medicamento, seguindo aprovações semelhantes do FDA americano (dezembro de 2025) e da EMA europeia.
Perguntas frequentes:
A partir de qual idade o Mounjaro pode ser usado em crianças?
A partir de 10 anos de idade, para o tratamento de diabetes tipo 2. Não há dados de segurança e eficácia para crianças menores de 10 anos.
O Mounjaro é indicado para crianças sem diabetes que têm sobrepeso ou obesidade?
Não. O medicamento não é aprovado para essa finalidade em crianças, mesmo que apresentem sobrepeso ou obesidade.
O Mounjaro é seguro para crianças?
Os estudos clínicos indicam que o medicamento é seguro e eficaz para crianças a partir de 10 anos com diabetes tipo 2, desde que utilizado sob prescrição e acompanhamento médico. O perfil de segurança foi consistente com o observado em adultos, embora com maior incidência de alguns efeitos gastrointestinais como vômitos e dor abdominal.
Quanto tempo leva para o medicamento fazer efeito?
As reduções significativas na hemoglobina glicada e no IMC foram observadas já nas primeiras 30 semanas de tratamento, com benefícios sustentados por até 52 semanas.
O medicamento está disponível no SUS?
A decisão da Anvisa autoriza o uso, mas a incorporação ao SUS depende de avaliação adicional pela Conitec (Comissão Nacional de Incorporação de Tecnologias no SUS). Atualmente, o Mounjaro está disponível na rede privada.
O que você achou dessa notícia? Comente, curta e compartilhe no perfil do Portal BomFm no Instagram. Sua opinião é importante para nós!
👉 Siga nosso Instagram:
Espaço para manifestação.
O Portal BomFm está à disposição da Anvisa, da Eli Lilly e das sociedades médicas de diabetologia para repercutir os desdobramentos da aprovação e eventuais atualizações sobre o uso do medicamento na população pediátrica brasileira.
Foto: science photo library.
Fonte: Portal BomFm com informações da Anvisa, The Lancet, FDA, NIH DailyMed, Healthline, Guia da Farmácia, PHARMASTAR e Patient Care Online.
Tags: BomFm, Saúde, Mounjaro, Tirzepatida, Anvisa, Diabetes Tipo 2, Saúde Infantil, Pediatria, Endocrinologia, Medicamentos, FDA, Eli Lilly, SURPASS-PEDS, Jornalismo, Informação, Google News.
Acompanhe o Portal BomFm em outros canais:
Receba as notícias em primeira mão com privacidade garantida: WhatsApp.
Acompanhe bastidores, notícias e interaja com a gente: Instagram.
Receba os principais destaques do dia: Google Notícias.
















COMENTÁRIOS